(著)山たー
メチルオレンジはpH指示薬として用いられます。メチルオレンジを水溶液にすると、酸性のときには赤色、塩基性のときには黄色を呈します。(以下の図はWikipediaよりお借りしました。)

それでは、この色の変化はどのように生じるのでしょうか。今回は量子化学計算の結果も踏まえて考えてみます。
※重いページになってしまいました。
分子の構造変化による吸収波長の変化
なぜ色の変化が生じるのかと調べると、初めに出てくるのは次のようなことです。メチルオレンジは中性・塩基性のときにベンゼノイド(benzenoid)構造を取り、酸性のときにキノイド(quinoid)構造を取ります(下図)。
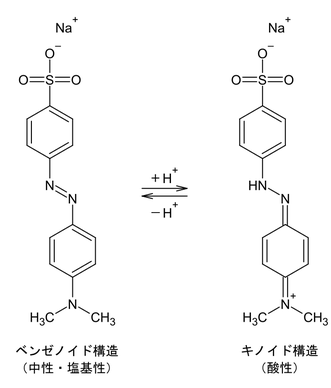
ベンゼノイド構造のときは黄色を呈し、キノイド構造のときは赤色を呈するということです。
HOMO-LUMOギャップ
それでは、なぜ構造変化により色の変化が生じるのでしょうか。HOMO-LUMOギャップを調べてみましょう。有機分子が呈色する場合、電子が励起するときのエネルギーに対応する波長の光を有機分子の電子が吸収することで、吸収光の補色が目に見えます。この基底状態と最低励起状態のエネルギー差はHOMO-LUMOギャップで近似できます(参考:有機化合物の構造と色)。
HOMO-LUMOギャップを調べるのは実際には間違っているのですが(参考:分子軌道とエネルギーギャップ)、近似としては考えられるということです。
以下にHF/6-31G(d)とB3LYP/6-31G(d)で計算したときのHOMO-LUMOギャップを示します。
HF/6-31G(d)
ベンゼノイド構造:9.4179eV
キノイド構造 :6.9580eV
B3LYP/6-31G(d)
ベンゼノイド構造:2.4817eV
キノイド構造 :0.8789eV

なお、色の変化が連続的なのはベンゼノイド構造とキノイド構造の比率の変化が連続的であるためです。
ギャップエネルギーの大きさに対するHOMO-LUMOの広がりの影響
ギャップエネルギーはキノイド構造の方が小さくなりました。この理由を考えましょう。まず、それぞれの構造におけるHOMOとLUMOを見てみましょう。以下はHF/6-31G(d)で計算した結果です(Isovalue=0.03)。
ベンゼノイド(benzenoid)構造:中性・塩基性
HOMO
LUMO
キノイド(quinoid)構造:酸性
HOMO
LUMO
画像にしたバージョンは次のようになります。

ここで箱の中の粒子と同じ考え方をしてみましょう(参考:なぜ非局在化で電子は安定化されるのか)。HOMOのオービタルの広がりが小さいと、HOMOのエネルギー準位は大きくなります。また、LUMOのオービタルの広がりが大きいと、LUMOのエネルギー準位は小さくなります。ゆえに、HOMOのオービタルの広がりが小さく、LUMOのオービタルの広がりが大きければ、ギャップエネルギーは小さくなります。
定量的ではないのですが、2つの構造のHOMOとLUMOを比べた時、キノイド構造のHOMOの広がりの方が大きいです。ただ、LUMOの広がりはあまり変わりません。
ということで、オービタルの広がりから色の変化が説明づけられたわけですが、ぶっちゃけ正しいかは微妙です。そもそもHOMOとLUMO
も「計算したらこうなりました」というだけなので、解決できているとは言い難いです。ただ、新しい説明の仕方ができたのではと思います。
コメントをお書きください